Câu 1. Magnesium (Mg) được sản xuất trong công nghiệp theo quá trình Pidgeon với nguyên liệu ban đầu là quặng dolomite. Quá trình được thực hiện qua các giai đoạn sau:
Giai đoạn 1: Nung quặng dolomite ở 900 - 1000oC.
MgCO3.CaCO3(s) MgO(s) + CaO(s) + 2CO2(g) ∆rH° = 279,9,0 kJ
Giai đoạn 2: Dùng Si trong ferrosilicon (Fe, Si) để tách Mg ở điều kiện chân không ở 1200 - 1500oC.
2MgO(s) + 2CaO(s) + Si(s) 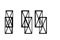 2Mg(g) + Ca2SiO4(s)
2Mg(g) + Ca2SiO4(s)
Phản ứng chung của quá trình Pidgeon là
2MgCO3.CaCO3(s) + Si(s) 2Mg(g) + Ca2SiO4(s) + 2CO2(g) ∆rH° = 183,0 kJ
a) Phản ứng chung của quá trình Pidgeon là phản ứng thu nhiệt.
b) Mg được tách theo phản ứng ở giai đoạn (2) thuộc phương pháp điện phân nóng chảy.
c) Phản ứng ở giai đoạn (1) thực hiện ở áp suất cao sẽ có hiệu suất cao hơn ở áp suất thường.
d) Nếu hiệu suất của quá trình là 90% thì cứ 1 tấn quặng dolomite (chứa 92% MgCO3.CaCO3(s) về khối lượng) sẽ điều chế được 108 kg kim loại magnesium.
Câu 2. Methylamine là một amine đơn giản, dễ bay hơi, dễ tan trong nước, được sử dụng làm nguyên liệu trong sản xuất dược phẩm, thuốc nhuộm, hoá chất nông nghiệp,...
Xét cân bằng của methylamine trong dung môi nước: 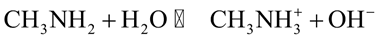
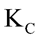
Trong khoảng nhiệt độ từ 10oC đến 50oC, sự phụ thuộc của vào nhiệt độ được biểu diễn ở đồ thị sau:
a) Theo thuyết Brønsted, methylamine là base do đã nhường proton của nước.
b) Ở nhiệt độ 25oC, giá trị nằm trong khoảng đến .
c) Tính base của methylamine tăng dần khi nhiệt độ tăng từ 10oC đến 50oC.
d) Phản ứng của methylamine với nước là phản ứng thu nhiệt.
7. LUYỆN ĐỀ BỨT PHÁ 9+ TỐT NGHIỆP THPT MÔN HÓA HỌC 2026 (Đề 7)