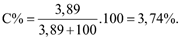Câu 3. Thực hiện thí nghiệm của kim loại nhóm IIA (M) với nước, độ tan (g/100g H2O ở 200C) của các hydroxide M(OH)2 tương ứng được ghi dưới bảng sau:
|
Hydroxide |
Be(OH)2 |
Mg(OH)2 |
Ca(OH)2 |
Sr(OH)2 |
Ba(OH)2 |
|
Độ tan (g/100g nước ) |
2,4.10-7 |
1,25.10-3 |
0,173 |
1,77 |
3,89 |
a) Qua độ tan của các hydroxide M(OH)2 có thể dự đoán mức độ phản ứng với nước của kim loại nhóm IIAcó xu hướng tăng dần từ Be tới Ba.
b) Giá trị pH của các dung dịch Ca(OH)2 0,01M, Sr(OH)2 0,01M và Ba(OH)2 0,01M xếp theo thứ tự tương ứng tăng dần.
c) Be(OH)2 có độ tan nhỏ nhất nên dễ tách khỏi bề mặt kim loại, do đó Be sẽ phản ứng với nước ngay điều kiện thường.
d) Ở 20 oC, nồng độ dung dịch Ba(OH)2 bão hòa là 3,84%.
Câu 4. Để tiết kiệm nguồn nguyên liệu hóa thạch, nhiều nước hiện nay đang lưu hành loại xăng sinh học E5. Giá trị E đề cập đến tỉ lệ phần trăm ethanol theo thể tích trong hỗn hợp nhiên liệu gồm ethanol và octane. Ví dụ, 1 lít xăng E5 gồm 50 mL ethanol (D = 0,789 g/cm3) và 950 mL octane (D = 0,703 g/cm3).
Cho phương trình nhiệt hóa học của phản ứng đốt cháy ethanol và octane:
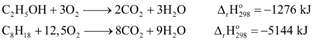
Một cách gần đúng, xem xăng thường chỉ là octane.
a) Ethanol trong xăng sinh học được sản xuất dựa vào quá trình lên men các nguồn carbohydrate có trong tự nhiên như tinh bột, glucose,…
b) Đốt cháy hoàn toàn cùng một lượng thể tích thì xăng E5 sẽ sinh ra ít khí carbon dioxide hơn so với xăng thường.
c) Đốt cháy hoàn toàn 2 lít xăng E5 tỏa ra một nhiệt lượng 62 540 kJ (làm tròn kết quả đến hàng đơn vị).
d) Trong quá trình bảo quản xăng E5, hàm lượng ethanol có thể bị giảm đi do hiện tượng hút ẩm từ không khí, dẫn đến tách lớp nhiên liệu.
10. LUYỆN ĐỀ BỨT PHÁ 9+ TỐT NGHIỆP THPT MÔN HÓA HỌC 2026 (Đề 10)