Câu 5. Trong sản xuất cao su buna-S (SBR), tỉ lệ mol giữa buta-1,3-diene và styrene thường dao động từ 70 : 30 đến 60 : 40.
Tại một nhà máy, để sản xuất ra loại cao su buna-S có tính năng linh hoạt và độ bền tốt, quá trình trùng hợp được thực hiện với số mol buta-1,3-diene gấp k lần styrene. Sau khi phản ứng kết thúc, thu được cao su buna-S có thành phần nguyên tố: 90,57%C và 9,43%H về khối lượng. Giá trị của k bằng bao nhiêu? (Làm tròn kết quả đến hàng phần mười)
Câu 6. Sự gia tăng các chất hữu cơ cũng gây suy giảm chất lượng nước. Để xác định chỉ số COD (Chemical Oxygen Demand, chỉ số quan trọng đánh giá chất lượng mẫu nước) của một mẫu nước thải hồ bơi, người ta dùng phương pháp chuẩn độ dichromate:
– Thí nghiệm với mẫu thử (nước thải): Lấy 25,0 mL mẫu nước thải cho vào bình nón, thêm chính xác 10,0 mL dung dịch K2Cr2O7 0,0167 M và lượng dư H2SO4 đặc. Đun sôi hồi lưu hỗn hợp để các chất hữu cơ bị oxi hóa hoàn toàn. Sau khi để nguội, chuẩn độ lượng K2Cr2O7 còn dư trong bình bằng dung dịch muối Mohr (NH4)2SO4.FeSO4.6H2O có nồng độ 0,10 M thì tiêu tốn hết 7,5 mL.
– Thí nghiệm với mẫu trắng (để đối chứng): Thay 25,0 mL nước thải bằng 25,0 mL nước cất tinh khiết, các bước làm tương tự như trên thì tiêu tốn hết 10,0 mL dung dịch muối Mohr (NH4)2SO4.FeSO4.6H2O có nồng độ 0,10 M.
Tính chỉ số COD của mẫu nước thải trên (đơn vị: mg O2/L). Biết quá trình oxi hóa của K2Cr2O7 tương đương với quá trình oxi hóa của O2.
10. LUYỆN ĐỀ BỨT PHÁ 9+ TỐT NGHIỆP THPT MÔN HÓA HỌC 2026 (Đề 10)
Câu 3. Có 4 ống nghiệm đựng Cu(OH)2 trong môi trường kiềm. Nhỏ từ từ vào từng ống nghiệm và khuấy đều dung dịch đựng các chất riêng rẽ sau: albumin, ethylamine, aniline, alanine. Có bao nhiêu ống nghiệm chứa chất hoà tan được Cu(OH)2?
Câu 4. Đồng là kim loại có thể tái chế nhiều lần những vẫn giữ nguyên đặc tính ban đầu. Năng lượng cần thiết để sản xuất 1 kg đồng từ quặng có thể dùng để tạo ra 10 kg đồng bằng con đường tái chế, do đó tái chế đồng tiết kiệm được x% năng lượng so với việc sản xuất đồng từ quặng. Giá trị của x là bao nhiêu?
10. LUYỆN ĐỀ BỨT PHÁ 9+ TỐT NGHIỆP THPT MÔN HÓA HỌC 2026 (Đề 10)
Câu 1. Reforming octane 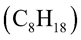 thu được các arene có công thức phân tử . Số công thức cấu tạo của các arene có cùng công thức phân tử là bao nhiêu?
thu được các arene có công thức phân tử . Số công thức cấu tạo của các arene có cùng công thức phân tử là bao nhiêu?
Câu 2. Tiến hành các thí nghiệm sau:
(1) Nhúng thanh đổng nguyên chất vào dung dịch FeCl3.
(2) Cắt miếng sắt tây (sắt tráng thiếc) để trong không khí ẩm.
(3) Nhúng thanh kẽm vào dung dịch H2SO4 loãng có nhỏ vài giọt dung dịch CuSO4.
(4) Quấn sợi dây đồng vào đinh sắt rồi nhúng vào cốc nước muối.
Trong các thí nghiệm trên, có bao nhiêu thí nghiệm chỉ xảy ra ăn mòn hoá học?
10. LUYỆN ĐỀ BỨT PHÁ 9+ TỐT NGHIỆP THPT MÔN HÓA HỌC 2026 (Đề 10)
Câu 3. Thực hiện thí nghiệm của kim loại nhóm IIA (M) với nước, độ tan (g/100g H2O ở 200C) của các hydroxide M(OH)2 tương ứng được ghi dưới bảng sau:
|
Hydroxide |
Be(OH)2 |
Mg(OH)2 |
Ca(OH)2 |
Sr(OH)2 |
Ba(OH)2 |
|
Độ tan (g/100g nước ) |
2,4.10-7 |
1,25.10-3 |
0,173 |
1,77 |
3,89 |
a) Qua độ tan của các hydroxide M(OH)2 có thể dự đoán mức độ phản ứng với nước của kim loại nhóm IIAcó xu hướng tăng dần từ Be tới Ba.
b) Giá trị pH của các dung dịch Ca(OH)2 0,01M, Sr(OH)2 0,01M và Ba(OH)2 0,01M xếp theo thứ tự tương ứng tăng dần.
c) Be(OH)2 có độ tan nhỏ nhất nên dễ tách khỏi bề mặt kim loại, do đó Be sẽ phản ứng với nước ngay điều kiện thường.
d) Ở 20 oC, nồng độ dung dịch Ba(OH)2 bão hòa là 3,84%.
Câu 4. Để tiết kiệm nguồn nguyên liệu hóa thạch, nhiều nước hiện nay đang lưu hành loại xăng sinh học E5. Giá trị E đề cập đến tỉ lệ phần trăm ethanol theo thể tích trong hỗn hợp nhiên liệu gồm ethanol và octane. Ví dụ, 1 lít xăng E5 gồm 50 mL ethanol (D = 0,789 g/cm3) và 950 mL octane (D = 0,703 g/cm3).
Cho phương trình nhiệt hóa học của phản ứng đốt cháy ethanol và octane:
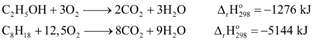
Một cách gần đúng, xem xăng thường chỉ là octane.
a) Ethanol trong xăng sinh học được sản xuất dựa vào quá trình lên men các nguồn carbohydrate có trong tự nhiên như tinh bột, glucose,…
b) Đốt cháy hoàn toàn cùng một lượng thể tích thì xăng E5 sẽ sinh ra ít khí carbon dioxide hơn so với xăng thường.
c) Đốt cháy hoàn toàn 2 lít xăng E5 tỏa ra một nhiệt lượng 62 540 kJ (làm tròn kết quả đến hàng đơn vị).
d) Trong quá trình bảo quản xăng E5, hàm lượng ethanol có thể bị giảm đi do hiện tượng hút ẩm từ không khí, dẫn đến tách lớp nhiên liệu.
10. LUYỆN ĐỀ BỨT PHÁ 9+ TỐT NGHIỆP THPT MÔN HÓA HỌC 2026 (Đề 10)
Câu 1. Cho thế điện cực chuẩn của các cặp oxi hóa – khử sau:
|
Cặp oxi hóa – khử |
Fe2+/Fe |
Fe3+/Fe2+ |
Cu2+/Cu |
Ag+/Ag |
|
Eo (V) |
–0,44 |
0,77 |
0,34 |
0,80 |
a) Fe3+ có tính oxi hóa mạnh hơn Cu2+ nhưng yếu hơn Ag+.
b) Tính khử của kim loại tăng dần theo thứ tự là Fe, Cu, Ag.
c) Sức điện động chuẩn lớn nhất của pin Galvani thiết lập từ hai cặp oxi hóa – khử trong số các cặp đã cho có giá trị là 1,57V.
d) Có thể làm sạch một mẫu bạc có lẫn các tạp chất là sắt và đồng bằng cách ngâm mẫu bạc trên vào một lượng dư dung dịch muối Fe3+.
Câu 2. á-amino acid Y là một amino acid thiết yếu, đóng vai trò quan trọng trong việc phục hồi cơ bắp. Cho biết:
– Y no, mạch hở, phân nhánh, phân tử chứa một nhóm amino và một nhóm carboxyl.
– Theo kết quả phân tích nguyên tố Y có 51,28% C.
a) Tổng số nguyên tử có trong một phân tử Y là 19.
b) Tên thay thế của Y là 2-aminopentanoic acid.
c) Ở điều kiện thường, Y là chất lỏng, dễ bay hơi và có vị ngọt.
d) Y di chuyển về cực âm khi đặt dung dịch Y ở pH = 6 trong điện trường.
10. LUYỆN ĐỀ BỨT PHÁ 9+ TỐT NGHIỆP THPT MÔN HÓA HỌC 2026 (Đề 10)