|
ĐỀ THI THAM KHẢO 5 (Đề thi có 05 trang) |
KÌ THI TỐT NGHIỆP THPT NĂM 2026 MÔN: HOÁ HỌC Thời gian làm bài: 50 phút, không kể thời gian phát đề
|
Họ, tên thí sinh: .....................................................................
Số báo danh: ..........................................................................
CẨM NANG LUYỆN ĐỀ BỨT PHÁ 9+ TỐT NGHIỆP THPT MÔN HÓA HỌC 2026 - FILE WORD CÓ LỜI GIẢI CHI TIẾT
- Tải MIỄN PHÍ file word kèm ma trận và lời giải chi tiết - Liên Hệ Zalo 0915347068
1. LUYỆN ĐỀ BỨT PHÁ 9+ TỐT NGHIỆP THPT MÔN HÓA HỌC 2026 (Đề 1)
2. LUYỆN ĐỀ BỨT PHÁ 9+ TỐT NGHIỆP THPT MÔN HÓA HỌC 2026 (Đề 2)
3. LUYỆN ĐỀ BỨT PHÁ 9+ TỐT NGHIỆP THPT MÔN HÓA HỌC 2026 (Đề 3)
4. LUYỆN ĐỀ BỨT PHÁ 9+ TỐT NGHIỆP THPT MÔN HÓA HỌC 2026 (Đề 4)
5. LUYỆN ĐỀ BỨT PHÁ 9+ TỐT NGHIỆP THPT MÔN HÓA HỌC 2026 (Đề 5)
6. LUYỆN ĐỀ BỨT PHÁ 9+ TỐT NGHIỆP THPT MÔN HÓA HỌC 2026 (Đề 6)
7. LUYỆN ĐỀ BỨT PHÁ 9+ TỐT NGHIỆP THPT MÔN HÓA HỌC 2026 (Đề 7)
Cho biết nguyên tử khối: H = 1, C = 12, N = 14, O = 16, Na = 23, Mg = 24, Al = 27, Zn = 65, Au = 197.
PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Nguyên tắc làm mềm nước cứng là làm giảm nồng độ của các ion nào sau đây?
A. Sulfate và chloride. B. Nitrate và hydrogencarbonate.
C. Magnesium và calcium. D. Sodium và potasium.
Câu 2. Xét cân bằng tổng hợp ammonia từ các đơn chất trong quá trình Haber:
Cân bằng sẽ chuyển dịch theo chiều thuận khi có tác động nào sau đây vào hệ?
A. Tăng nồng độ ammonia. B. Tăng áp suất chung.
C. Tăng nhiệt độ. D. Tăng áp suất ammonia.
Câu 3. Nguyên tử Ti có cấu hình electron là [Ar] 3d24s2. Số electron hóa trị trong nguyên từ Ti là
A. 3. B. 2. C. 1. D. 4.
Câu 4. Ethanol (C2H5OH) được sử dụng làm đồ uống có cồn, nhiên liệu, chất khử khuẩn; còn diethyl ether (CH3OCH3) được dùng làm dung môi và có khả năng gây mê. Ethanol và diethyl ether là hai hợp chất
A. đồng đẳng. B. đồng phân cấu tạo.
C. đồng phân hình học. D. đồng vị.
Câu 5. Cho các cân bằng giữa các dạng tồn tại của glycine trong dung dịch nước như sau:
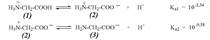
Dựa vào các cân bằng trên, nhận xét nào sau đây đúng?
A. Lực acid của nhóm -COOH lớn hơn lực acid của nhóm -NH3+.
B. Lực base của nhóm -COO– lớn hơn nhóm -NH2.
C. Dạng (1) là dạng tồn tại chủ yếu trong môi trường base.
D. Trong dung dịch HCl, dạng (2) tồn tại chủ yếu.
Câu 6. Ngoài dạng mạch hở, glucose tồn tại chủ yếu ở hai dạng mạch vòng là -glucose và -glucose. Trong vòng glucose, nguyên tử carbon số mấy nằm ngoài cấu trúc vòng sáu cạnh?
A. Carbon số 1. B. Carbon số 2. C. Carbon số 6. D. Carbon số 3.
Câu 7. Nhiệt độ ngọn lửa (flame temperature) là nhiệt độ cao nhất tạo ra bởi phản ứng đốt cháy chất cháy ở áp suất khí quyển. Nhiệt độ ngọn lửa phản ánh mức độ toả nhiệt của phản ứng đốt cháy và thường được xác định bằng lí thuyết.
Phát biểu nào sau đây là sai?
A. Phản ứng đốt cháy nhiên liệu thường kèm theo toả nhiệt mạnh và tạo ra nhiệt độ ngọn lửa cao.
B. Quá trình cháy của ethanol tạo nhiệt độ ngọn lửa cao nên dễ gây bỏng.
C. Đèn xì oxygen - acetylen dùng trong hàn cắt kim loại do tạo ra được nhiệt độ ngọn lửa cao trên .
D. Khi hoả hoạn, nhiệt độ ngọn lửa càng thấp càng có nguy cơ bùng phát đám cháy mạnh.
Câu 8. Trong các amine sau: ethylamine, propylamine, dimethylamine và methylamine, chất có nhiệt độ sôi cao nhất là
A. ethylamine. B. propylamine. C. dimethylamine. D. methylamine.
Câu 9. Phản ứng thuỷ phân hoàn toàn tinh bột trong môi trường acid tạo thành glucose thuộc loại phản ứng
A. tăng mạch polymer. B. giữ nguyên mạch polymer.
C. cắt mạch polymer. D. tổng hợp polymer.
Câu 10. Phát biểu nào sau đây không đúng?
A. Nylon-6,6 thuộc loại tơ tổng hợp.
B. Thành phần của vật liệu composite chỉ chứa polymer.
C. Tơ tằm thuộc loại tơ thiên nhiên.
D. Cao su là những vật liệu polymer có tính đàn hồi.
Câu 11. Thiết lập một pin Galvani ở điều kiện chuẩn từ hai cặp oxi hoá - khử là và . Phát biểu nào sau đây về pin Galvani trên là đúng?
A. Pin Galvani có anode bằng Pb, cathode bằng Fe.
B. Ở anode xảy ra quá trình .
C. Sức điện động của pin là .
D. Dòng điện trong pin chạy từ cực Pb sang cực Fe.
Câu 12. Tiến hành điện phân dung dịch bằng dòng điện một chiều (với điện cực trơ). Cho các quá trình sau:
(a) ; (b) .
(c) ; (d) .
Quá trình xảy ra ở anode và cathode lần lượt là
A. (d) và (a). B. (a) và (b). C. (b) và (c). D. (c) và (d).
Câu 13. Khi cho kim loại X tác dụng với dung dịch H2SO4 (loãng) hoặc với dung dịch H2SO4 (đặc, nguội) đều chỉ thu được một loại muối sulfate. Kim loại phù hợp với X là
A. Al. B. Fe. C. Cu. D. Mg.
Câu 14. Phương pháp nhiệt luyện dùng các chất khử như để khử các oxide kim loại ở nhiệt độ cao thành kim loại. Quá trình nào sau đây tách kim loại bằng phương pháp nhiệt luyện?
A. Tách sắt từ quặng hematite. B. Tách nhôm từ quặng bauxite.
C. Tách sodium từ muối ăn. D. Tách đồng từ copper(II) sulfate.
Câu 15. Các kim loại nhóm IA có độ cứng thấp (đều mềm, có thể cắt bằng dao, kéo) là do nguyên nhân chính nào sau đây?
A. Tính kim loại mạnh. B. Thế điện cực chuẩn rất âm.
C. Liên kết kim loại yếu. D. Cấu trúc mạng tinh thể đặc khít.
Câu 16. Trong phòng thí nghiệm, ion Ba2+ trọng duñg dịch được nhận biết bằng phương pháp hoá học với thuốc thử là dung dịch chứa ion
A. . B. . C. . D. .
Câu 17. Nguyên tố kim loại thuộc dãy chuyển tiếp thứ nhất, có trong hemoglobin (chất vận chuyển oxygen cho các tế bào) và myoglobin (chất dự trữ oxygen cho cơ thể) là
A. sắt. B. đồng. C. nickel. D. chromium.
Câu 18. Cho hợp chất hữu cơ X có công thức cấu tạo như sau:
Thuỷ phân X trong môi trường NaOH, thu được hai sản phẩm hữu cơ là Y và . Nhận định nào sau đây là sai?
A. X là hợp chất hữu cơ đa chức. B. X thuộc loại carbohydrate.
C. Z có tính chất của polyalcohol. D. Y được dùng để sản xuất xà phòng.
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1. Saccharose được cấu tạo từ một đơn vị α-glucose và một đơn vị β-fructose. Công thức cấu tạo của saccharose mô ta như hình bên.
a) Saccharose là một disaccharide có công thức phân tử là C12H20O11.
b) Các đơn vị α-glucose và β-fructose liên kết với nhau qua liên kết α-1,2-glycoside.
c) Saccharose không còn nhóm -OH hemiacetal nên chỉ tồn tại ở dạng mạch vòng
d) Saccharose có khả năng tham gia phản ứng với thuốc thử Tollens.
Câu 2. Trong phòng thí nghiệm, một học sinh thực hiện thí nghiệm sau:
Bước 1: Cho từ từ dung dịch vào ống nghiệm đựng dung dịch , lúc đầu xuất hiện phức chất trung hoà X màu xanh lá cây, có dạng hình học bát diện, chỉ chứa phối tử và .
Bước 2: Thêm tiếp dung dịch đến dư, thu được phức chất bát diện Y có màu xanh dương, chỉ - chứa phối tử .
a) Công thức cấu tạo của X là .
b) Liên kết giữa phối tử và nguyên tử trung tâm trong X và Y là liên kết ion.
c) Công thức cấu tạo của Y là .
d) Dấu hiệu nhận biết Y được tạo thành là có sự hoà tan kết tủa.
Câu 3. Nhôm được sử dụng phổ biến để sản xuất các thiết bị, dụng cụ, đồ gia dụng do có nhiều tính chất ưu việt như dẻo, nhẹ, dẫn điện, dẫn nhiệt tốt, chịu ăn mòn hoá học khá tốt.
Thí nghiệm đo tốc độ ăn mòn của nhôm trong môi trường dung dịch HCl 2 M:
Nhúng một miếng nhôm hình lập phương có diện tích toàn phần đã được làm sạch vào dung dịch HCl 2 M (nồng độ không đổi) ở nhiệt độ . Sau t (giờ) giờ, khối lượng miếng nhôm giảm .
Tốc độ ăn mòn (mm/năm) của miếng nhôm được tính theo công thức: .
Trong đó: là khối lượng riêng của nhôm.
Trong cùng điều kiện thí nghiệm, tốc độ ăn mòn của kẽm là mm/năm.
a) Nhôm là kim loại có tính khử mạnh nhưng có khả năng tự bảo vệ bằng cách hình thành lớp oxide mỏng để chống ăn mòn.
b) Tốc độ ăn mòn của nhôm trong điều kiện thí nghiệm trên là mm/năm..
c) Kẽm có tốc độ ăn mòn lớn hơn nhôm do kẽm có tính khử mạnh hơn nhôm.
d) Nhôm và kẽm đều được sử dụng để mạ kim loại bằng phương pháp điện phân.
Câu 4. Hợp chất hữu cơ đơn chức X có mùi thơm của quả dứa chín và được sử dụng trong tổng hợp dược phẩm,... Kết quả phân tích nguyên tổ cho thấy X có %C = 58,82%, %H = 9,80% (về khối lượng), còn lại là oxygen. Trên phổ MS của X thấy xuất hiện peak của ion phân tử có giá trị m/z = 102. Trên phổ IR của X thấy xuất hiện tín hiệu đặc trưng ở 1740 cm-1.
Cho bảng tín hiệu phổ hồng ngoại (IR) của một số loại liên kết:
|
Hợp chất |
Loại liên kết |
Số sóng (cm-1) |
|
Aldehyde |
C = O |
1740 – 1720 |
|
C – H |
2900 – 2700 |
|
|
Carboxylic acid |
C = O |
1725 – 1700 |
|
O – H |
3300 – 2500 |
|
|
Ester |
C = O |
1750 – 1735 |
|
C – O |
1300 – 1000 |
|
|
Ketone |
C = O |
1725 – 1700 |
a) Phân tử X có tỉ lệ số nguyên tử carbon và hydrogen là 1 : 2.
b) X là carboxylic acid no, đơn chức, có công thức phân tử C5H10O2.
c) Ở điều kiện thường, X phản ứng với NaOH với tỉ lệ mol là 1 : 1.
d) X tạo được liên kết hydrogen với nước nên X tan tốt trong nước ở điều kiện thường.
PHẦN III: Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Một mẫu polystyrene (PS) được dùng làm hộp xốp bảo quản thực phẩm có chứa hỗn hợp gồm nhiều đoạn mạch PS có số mắt xích khác nhau và có phân tử khối trung bình là 210 600. Tính số mắt xích trung bình của mẫu PS đó.
Câu 2. Cho dãy các kim loại: Li, Na, Al, Ca, Mg và Rb. Có bao nhiêu kim loại kiềm trong dãy kim loại trên?
Câu 3. Cho các chất giặt rửa ở cột (I) và các ưu điểm và nhược điểm ở cột (II) sau
|
Cột (I) |
Cột (II) |
||
|
1) |
Xà phòng |
a) |
Ưu điểm: lành tính với da, dễ phân hủy bởi vi sinh vật nên không gây ô nhiễm môi trường. Nhược điểm: Giá thành cao, khó sản xuất ở quy mô công nghiệp. |
|
2) |
Chất giặt rửa tổng hợp |
b) |
Ưu điểm: Dùng được với nước cứng. Giá thành thấp. Nhược điểm: có gốc hydrocarbon phân nhánh hoặc chứa vòng benzene sẽ gây ô nhiễm môi trường do chúng rất khó bị vi sinh vật phân hủy. |
|
3) |
Chất giặt rửa tự nhiên |
c) |
Ưu điểm: có thể bị phân hủy bởi vi sinh vật nên ít gây ô nhiễm môi trường. Nhược điểm: khi dùng với nước cứng tạo ra kết tủa bám trên bề mặt vải, ảnh hưởng đến chất lượng vải, đồng thời làm giảm tác dụng giặt rửa. |
Hãy ghép các thông tin của cột (II) với cột (I) phù hợp với thứ tự a), b), c) thành một dãy ba chữ số (ví dụ: 132, 213,…).
Câu 4. Xét hai giai đoạn đầu trong kĩ thuật tách vàng từ quặng bằng phương pháp cyanide.
Giai đoạn 1: Ngâm quặng vàng trong dung dịch NaCN rồi sục không khí liên tục để chuyển vàng thành hợp chất tan:
4Au + 8NaCN + O2 + 2H2O → 4Na[Au(CN)2] + 4NaOH
Giai đoạn 2: Tách vàng từ dung dịch bằng phương pháp thủy luyện:
2Na[Au(CN)2] + Zn → Na2[Zn(CN)4] + 2Au
Trong giai đoạn 2, để tạo ra 394 kg vàng người ta đã sử dụng m kg kẽm, biết kẽm dùng dư 10% so với lượng cần thiết. Giá trị của m bằng bao nhiêu? (Kết quả làm tròn đến hàng phần mười).
Câu 5. Chuẩn độ hàm lượng ion Fe2+ trong môi trường acid (chứa trong bình tam giác) bằng dung dịch KMnO4 đã biết nồng độ (chứa trên burette). Trong quá trình chuẩn độ, nếu dung dịch trên burette được thêm vào bình tam giác quá nhanh thì trong bình sẽ xuất hiện kết tủa nâu MnO2 theo phương trình hóa học dưới đây, dẫn đến sai lệch kết quả chuẩn độ:
MnO4–(aq) + H+(aq) + Fe2+(aq) → MnO2(s) + Fe3+ + H2O(l)
Giả sử một học sinh thao tác chuẩn độ sai, làm 55% lượng MnO4– chuẩn độ chuyển thành MnO2 (phần còn lại vẫn phản ứng tạo Mn2+), tổng lượng Fe2+ bị oxi hóa là 2,4 mmol. Thể tích dung dịch KMnO4 0,02M đã dùng tăng bao nhiêu mL so với khi chuẩn độ với thao tác phù hợp? (Kết quả làm tròn đến hàng phần trăm)
Câu 6. Một Trạm Y tế vùng sâu sử dụng máy phát điện chạy bằng xăng E10 (gồm ethanol, heptane, octane, theo tỉ lệ số mol) để cung cấp điện khi mất nguồn lưới. Khi đốt cháy hoàn toàn, 1 mol mỗi chất trong xăng E10 giải phóng nhiệt lượng như sau:
|
Chất |
Ethanol |
Heptane |
Octane |
|
|
1365 |
4820 |
5460 |
Biết rằng năng lượng bị mất vào môi trường và máy phát điện cần 48000 kJ hữu ích mỗi giờ để vận hành. Nếu dùng xăng E10, thì máy có thể hoạt động liên tục trong khoảng thời gian là bao nhiêu giờ? (Làm tròn đến hàng phần trăm)
------------------------- HẾT -------------------------
- Thí sinh không sử dụng tài liệu.
- Giám thị không giải thích gì thêm.
|
ĐỀ THAM KHẢO SỐ 5
|
KÌ THI TỐT NGHIỆP THPT NĂM 2026 MÔN: HÓA HỌC
|
Phần I: Mỗi câu trả lời đúng được 0,25 điểm
|
Câu |
Đáp án |
Câu |
Đáp án |
|
1 |
C |
10 |
B |
|
2 |
B |
11 |
C |
|
3 |
D |
12 |
A |
|
4 |
A |
13 |
D |
|
5 |
A |
14 |
A |
|
6 |
C |
15 |
C |
|
7 |
D |
16 |
C |
|
8 |
B |
17 |
A |
|
9 |
C |
18 |
B |
Phần II: Điểm tối đa của 01 câu hỏi là 1 điểm
- Thí sinh chỉ lựa chọn chính xác 01 ý trong 1 câu hỏi được 0,1 điểm;
- Thí sinh chỉ lựa chọn chính xác 02 ý trong 1 câu hỏi được 0,25 điểm;
- Thí sinh chỉ lựa chọn chính xác 03 ý trong 1 câu hỏi được 0,5 điểm;
- Thí sinh lựa chọn chính xác cả 04 ý trong 1 câu hỏi được 1 điểm;
|
Câu |
1 |
2 |
3 |
4 |
|
Đáp án |
a) Sai b) Đúng c) Đúng d) Sai |
a) Sai b) Sai c) Đúng d) Đúng |
a) Đúng b) Sai c) Sai d) Sai |
a) Đúng b) Sai c) Sai d) Sai |
Phần III: Mỗi câu trả lời đúng được 0,25 điểm
|
Câu |
1 |
2 |
3 |
4 |
5 |
6 |
|
Đáp án |
2025 |
3 |
321 |
71,5 |
6,77 |
1,84 |
HƯỚNG DẪN GIẢI MÃ ĐỀ THI 500
PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Nguyên tắc làm mềm nước cứng là làm giảm nồng độ của các ion nào sau đây?
A. Sulfate và chloride. B. Nitrate và hydrogencarbonate.
C. Magnesium và calcium. D. Sodium và potasium.
Câu 2. Xét cân bằng tổng hợp ammonia từ các đơn chất trong quá trình Haber:
Cân bằng sẽ chuyển dịch theo chiều thuận khi có tác động nào sau đây vào hệ?
A. Tăng nồng độ ammonia. B. Tăng áp suất chung.
C. Tăng nhiệt độ. D. Tăng áp suất ammonia.
Câu 3. Nguyên tử Ti có cấu hình electron là [Ar] 3d24s2. Số electron hóa trị trong nguyên từ Ti là
A. 3. B. 2. C. 1. D. 4.